신약, 개량신약 등의 연구개발(R&D) 성과로 이익을 창출하고 벌어들인 수익을 R&D에 재투자하는 R&D 선순환 구조가 빛을 발하며 수익성 개선에 크게 기여했다는 평가다.
올해는 특히 자체 개발한 국산 의약품들의 선전과 더불어 롤론티스, 포지오티닙 등 FDA(미국 식품의약국) 시판허가가 기대되고 있어 성장세에 더욱 탄력이 붙을 것으로 전망되고 있다.
13일 금융감독원 전자공시시스템에 따르면 한미약품의 지난해 연결 매출은 1조2032억 원으로 전년에 비해 11.8% 늘었고, 영업이익은 1254억 원으로 156.1% 성장했다. 이에 따른 영업이익률은 10.4%로 전년 대비 5.9%포인트 상승한 것으로 집계됐다.
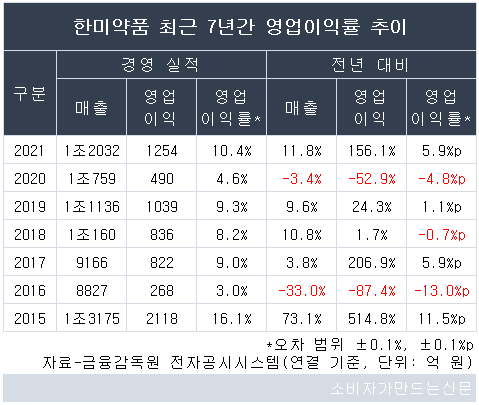
이후 줄곧 3~9%대에 머물다 지난해 시장 예상치를 웃도는 깜짝 실적을 기록했다. 매출과 영업이익을 모두 늘렸는데 특히 영업이익이 세 자릿수 비율로 급성장했다.
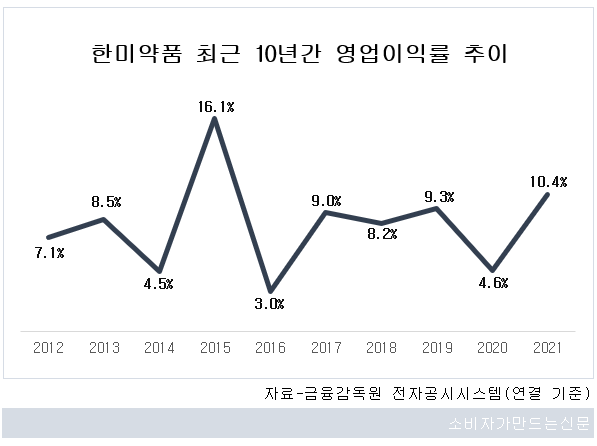
기술수출도 이익 증가에 한몫 했다. 지난해 1월 에퍼메드와 1억4500만 달러 규모의 안과 분야 혁신신약 루미네이트 라이선스 계약을, 같은 해 11월 앱토즈와 4억2000만 달러 규모의 급성골수성 백혈병 혁신신약 HM43239 라이선스 계약을 체결하면서 200억 원이 넘는 계약금이 4분기에 반영됐다.
이 같은 성장 기저에는 R&D 재원의 선순환 구조가 깔려있다는 분석이다.
한미약품은 지주사 체제 전환을 위해 인적 분할을 실시한 2010년 7월부터 지난해까지 매출 대비 연구개발 비율을 한해도 거르지 않고 매년 10%대 이상으로 유지하며 R&D 선순환 고리를 발 빠르게 구축했다는 평가를 받아왔다.
자체 개발한 품목들은 마진을 많이 남겼고 이렇게 벌어들인 재원은 R&D에 다시 투자됐다. 코로나19 펜데믹으로 어려운 영업환경 속에서 한미약품이 크게 선전할 수 있었던 배경이다.
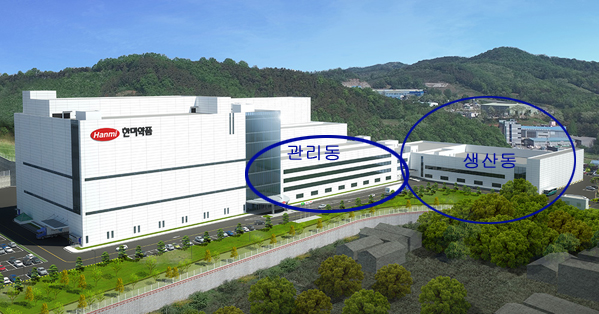
공장 내에 위치한 연구개발센터와 생산동의 지리적 이점도 눈여겨볼 만하다.
한미약품의 케미컬 의약품 공장인 팔탄 스마트플랜트는 단순 생산 작업을 반복하지 않는다. 생산동 바로 옆에 제제연구센터인 관리동이 위치해 실험실에서 연구한 결과물을 공장으로 직접 가져가서 생산에 바로 적용할 수 있다.
바이오 의약품 공장인 바이오플랜트도 마찬가지다. 생산동과 품질관리동이 붙어 있어 연구개발과 실험 생산이 동시 가능하다는 장점이 있다. 이 같은 설비 전략은 연구개발 마중물 역할을 하며 아모잘탄 패밀리, 롤론티스 등의 자체 개발 신약 탄생에 일조했다.
금융정보업체 에프앤가이드에 따르면 한미약품의 올해 예상 매출은 1조2785억 원으로 전년에 비해 6.3% 늘고, 영업이익은 1334억 원으로 6.4% 성장할 것으로 분석됐다. 이에 따른 영업이익률은 10.43%로 지난해보다 0.01%포인트 상승할 것으로 보인다.
올해는 신약과 관련한 각종 호재도 예상된다. FDA는 미국 현지시각 11일 차세대 장기지속형 호중구감소증 바이오신약 롤론티스의 시판허가 신청서(BLA, Biologics License Application)를 승인하고 시판 허가를 위한 공식 심사 절차에 착수했다.
또 다른 항암 혁신신약인 포지오티닙의 연내 FDA 시판허가 승인도 기대되는 상황이다. 올해 2월 FDA로부터 신약 시판허가 신청서(NDA, New Drug Application)를 승인받았다. 처방의약품 신청자 수수료 법(Prescription Drug User Fee Act, PDUFA)에 따라 오는 11월 24일 안으로 최종 허가 여부가 결정될 예정이다.
특히 포지오티닙은 세상에 없는 혁신신약(First In Class)으로 개발됐다. 현재까지 포지오티닙과 동일한 적응증으로 FDA가 승인한 치료제는 없다. 포지오티닙은 지난해 3월 FDA로부터 패스트 트랙(Fast Track)으로 지정받기도 했다.
대신증권 임윤진 애널리스트는 지난 달 21일 발표한 리포트에서 "롤론티스와 포지오티닙 두 약물 모두 국내 생산시설 현장 실사가 최종 허가여부에 중요하게 작용할 것으로 예상된다. 포지오티닙의 경우 HER2 Exon 20 변이 비소세포폐암에 대한 상용화된 치료제가 없어 허가 가능성이 긍정적이라 할 수 있다"고 말했다.
[소비자가만드는신문=김경애 기자]



