셀트리온(대표 서진석)이 2030년까지 바이오시밀러 18개 제품을 확보하겠다는 목표 달성을 향해 순항하고 있는 것으로 나타났다.
14일 업계에 따르면 셀트리온이 보유한 바이오시밀러는 목표 제시 전인 2023년 6종에서 현재 11종으로 5개 늘었다.
당시 파이프라인으로 제시됐던 옴리클로, 스테키마부터 앱토즈마까지 5종의 파이프라인 모두 2024년 중 허가를 받는 데 성공했다.
현재 개발 중인 바이오시밀러 파이프라인의 연구 및 임상시험이 차질없이 이뤄지면 목표는 무난히 달성할 것으로 기대된다.
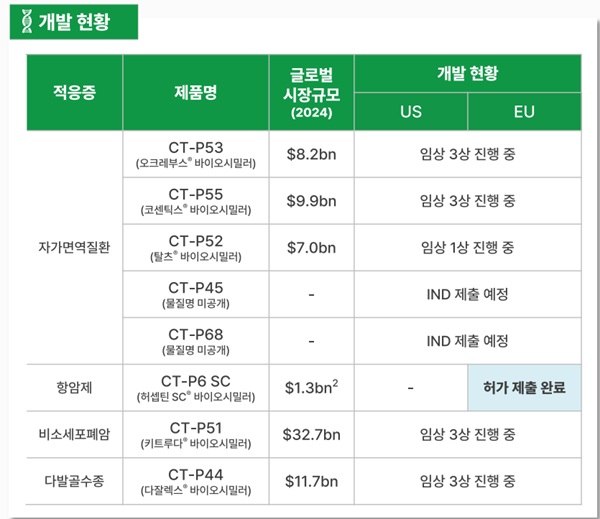
셀트리온이 개발 단계를 공개한 바이오시밀러 파이프라인은 8종이다. △CT-P44 △CT-P51 △CT-P53 △CT-P55 등 4종이 임상 3상 단계로 상업화를 눈앞에 두고 있다.
‘CT-P52’가 임상 1상을 진행 중이고, 허쥬마의 피하주사(SC) 제형인 ‘CT-P6 SC’는 허가 신청을 마쳤다. ‘CT-P45’와 ‘CT-P68’은 임상시험승인계획서(IND) 제출이 예정돼 있다.
셀트리온은 2023년 상반기 실적발표 자료를 통해 당시 자가면역질환 치료제 ‘램시마’, 항암제 ‘허쥬마’와 ‘트룩시마’ 등 6개였던 바이오시밀러 제품군을 2030년 22개로 늘리겠다는 중장기 목표치를 제시했다.
이후 셀트리온은 항체-약물접합체(ADC) 항암 신약 개발, 미국 생산시설 인수 등에 투자하면서 중장기 성장 로드맵을 조정했다. 2025년 초 JP모건 헬스케어 컨퍼런스에서 ADC, 다중항체 신약을 차세대 성장 축으로 제시하며 바이오시밀러에 집중하던 사업구조에서 신약개발 기업으로 나아가겠다는 비전을 제시했다.
그해 11월 일라이 릴리의 미국 뉴저지주 브랜치버그 바이오의약품 생산시설 인수 계약 직후 새로운 중장기 성장 목표를 제시했다.
당시 서정진 회장은 2030년까지 18개 바이오시밀러 제품 상업화 이후 2038년까지 41개 출시를 목표로 진행한다고 밝혔다. 이에 따라 제품군이 타깃하는 시장 규모는 11개인 현재 85조 원에서 2030년 274조, 2038년 408조 원까지 확대될 것으로 기대했다.
셀트리온 관계자는 “글로벌 제약 시장 환경 변화와 신약 파이프라인 확대 등을 종합적으로 고려해 당사의 중장기 사업 전략을 설정했다. 종전 계획보다 바이오시밀러와 신약 파이프라인의 전체 개발 품목은 더 확대됐으며 특히 바이오시밀러의 경우 2038년까지 41개로 확대될 예정”이라고 말했다.
셀트리온의 사업구조가 다변화하면서 바이오시밀러에 집중하던 개발 역량을 분산한 것으로 풀이된다. 실제 셀트리온은 신약 개발 부문에서 2027년까지 10종 이상 임상 단계 진입을 포함해 총 20종 파이프라인을 구축한다는 목표를 추진 중이다.
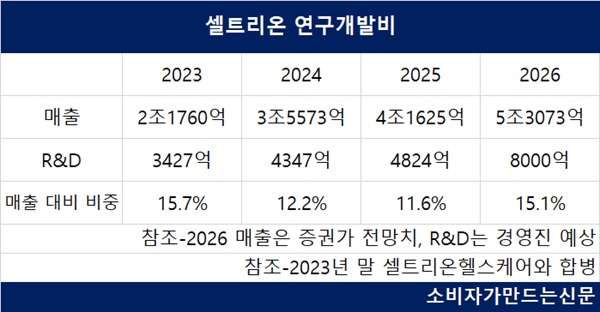
셀트리온의 연구개발비는 매년 증가세에 있지만 특히 올해는 더욱 눈에 띄게 증가할 전망이다. 올해 셀트리온의 예상 R&D 규모는 8000억 원이다. 2027년에는 1조 원을 기록할 것으로 보인다.
매출 대비 연구개발비 비중도 매년 두 자릿수 비율을 기록 중이다.
바이오시밀러 목표 달성 가능성을 높이는 외부 변수도 있다. 미국 식품의약국(FDA), 유럽의약품청(EMA) 등 글로벌 규제기관이 바이오시밀러 개발 과정에서 임상자료 부담을 줄이고 개발 단계를 줄이는 방향으로 제도를 손질하고 있기 때문이다.
실제 셀트리온이 임상 3상을 진행 중인 CT-P51의 경우 지난달 24일 식품의약품 안전처로부터 대상 환자 수가 기존 606명에서 220명으로 하는 임상시험변경계획 승인을 받았다. 2월에는 EMA으로부터 CT-P55의 환자수를 375명에서 153명으로 조정하는 계획을 승인 받았다. 이 같은 규제 완화 흐름은 셀트리온에게 비용과 기간을 줄이는 요인으로 작용할 수 있다.
[소비자가만드는신문=정현철 기자]



